【技术干货】FDA DMF备案意义在哪?看ACRO蛋白如何助力CAR-T项目申报
DMF是什么?
药品主文件(Durg Master Files, DMF)是持有者递交给FDA的药物存档文件,包含药物产品在生产、操作、包装和储存过程中用到的设施、操作流程、原料等保密细节信息[1]。
为什么要进行FDA DMF备案?
根据美国联邦食品、药品和化妆品法规定,药品在上市之前申报者必须向FDA提出相关的申请,比如临床研究申请(IND)、新药注册(NDA)和生物制品许可证申请(BLA)等,并需要提供该药物在安全性、有效性和质量三方面的全部信息[2],其中涉及到原料药、辅料的相关技术内容,但是准备这些材料无疑会耗费大量的时间和精力,同时原料供应商也不愿透漏自己的技术信息,因此严重影响临床申报的进程。
为解决这一问题,FDA建立了DMF体系,原料供应商以DMF文件的形式将所需的技术内容直接交给FDA备案并获得备案编号,药物申报者可以直接使用DMF备案编号来代替申报过程中需要提供有关原料和辅料的具体信息[3],极大程度上缩短了审查和评估时间。
ACROBiosystems自主开发的CD19和BCMA蛋白系列产品已完成美国FDA DMF备案(FDA DMF编号:034936),您的CAR-T细胞治疗研究项目进行临床申请或新药注册的监管备案文件中可直接引用我们的DMF编号,从而节约产品审查和评估时间,缩减新药临床申报的准备工作。
ACRO DMF备案产品列表
如果您有其他产品的FDA DMF备案需求,请点击下方联系我们
如何引用我们的DMF编号授权
如果您使用了ACRO的DMF备案系列产品并需要引用DMF编号,点击下方按钮向ACRO提出授权申请,收到申请后,我们将向FDA提供DMF授权书。
> 覆盖非标记、荧光标记和生物素标记蛋白多种形式
> 蛋白活性经Flow cytometry、SPR、ELISA验证
> 适用于CAR表达检测和抗体药筛选
> 蛋白活性经Flow cytometry、SPR、ELISA验证
> 适用于CAR表达检测和抗体药筛选
产品数据
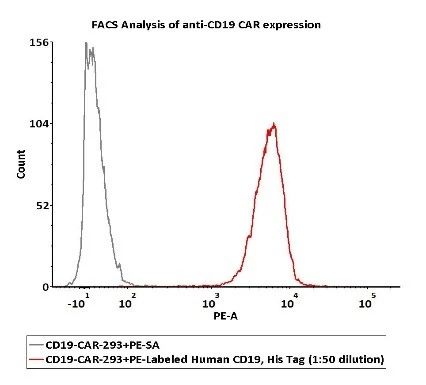
经流式验证PE-Labeled CD19蛋白能够特异性检测Anti-CD19 CAR 表达
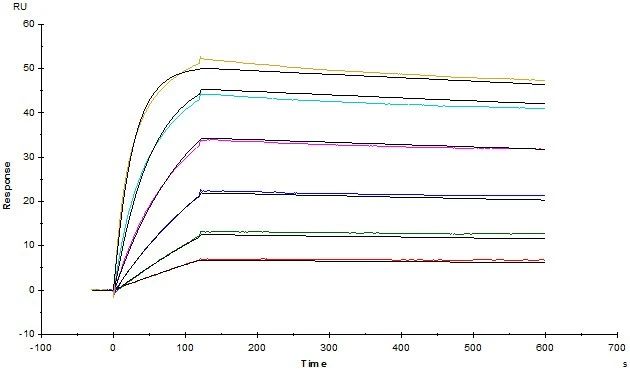
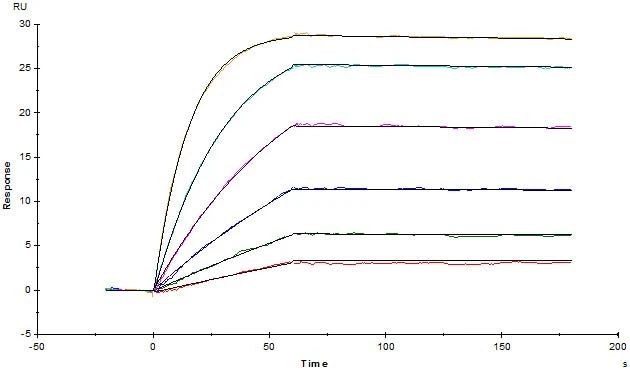
经SPR验证Human CD19蛋白的亲和力常数为0.17 nM
FITC-Labeled Human BCMA流式检测Anti- BCMA CAR表达

经SPR验证Human BCMA蛋白的亲和力常数为0.388 nM
更多CAR-T靶点蛋白系列产品
> 全部CAR-T靶点蛋白产品> CD19蛋白产品
> CD22蛋白产品
> MSLN蛋白产品
> 抗FMC63抗体产品
参考文献:
[1] https://www.fda.gov/drugs/forms-submission-requirements/drug-master-files-dmfs
[2] Federal Food Drug and Cosmetic Act
[3] https://www.fda.gov/drugs/guidances-drugs/drug-master-files-guidelines