- English
- 日本語
- 한국어
- Deutsch
- Français
- Español
No data
官方服务号
招聘公众号
| Product Details | Cat. No. | Unit Definition |
|---|---|---|
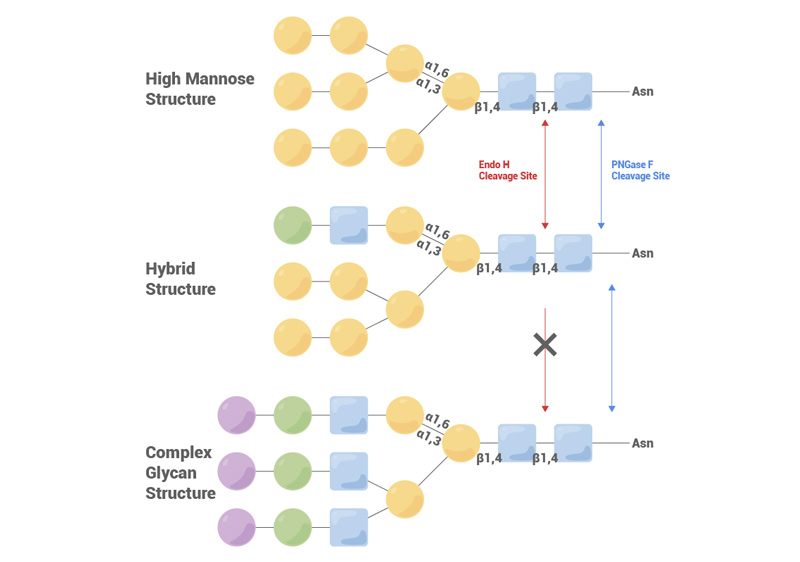
| Endo H (500U/μl) | ENH-S5116 | One unit is defined as the amount of enzyme required to remove >95% of the carbohydrate from 10µg of denatured RNase B in 1 hour at 37°C in a total reaction volume of 10µl. |
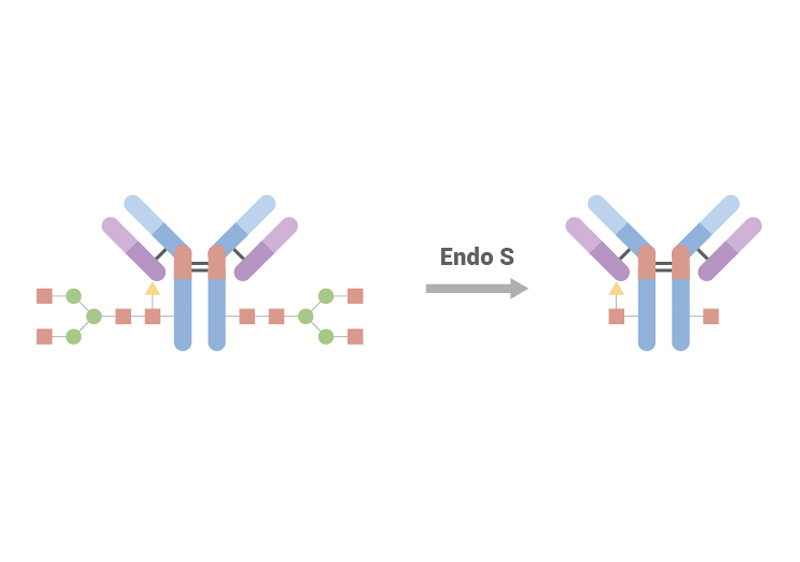
| Endo S (200U/μl) | ENS-S5143 | One unit deglycosylates ≥ 95% of 1 μg human IgG, when incubated in 10 mM sodium phosphate, 150 mM NaCl, pH7.4 at 37°C for 30 min. |
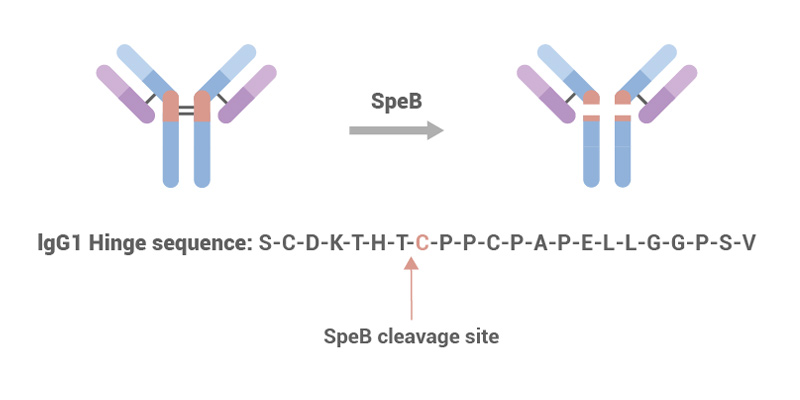
| SpeB (40U/μl) | SPB-S5115 | One unit digests ≥ 95% of 1 µg human IgG1 when incubated in PBS ith 5 mM DTT or TCEP, pH 7.4 at 37°C for 1 hour. |
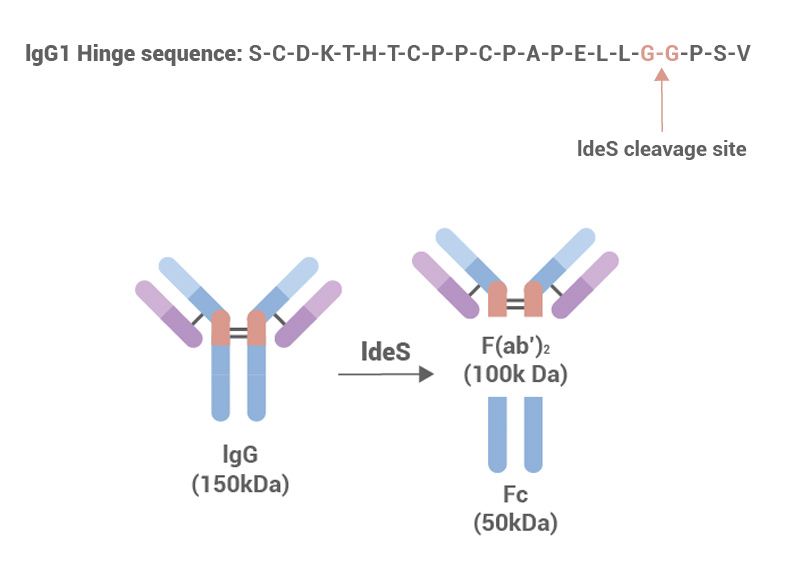
| IdeS (20U/μl) | IDS-S5143 | One unit digests ≥ 95% of 1 μg human IgG when incubated in 10 mM sodium phosphate, 137 mM NaCl, 2.7 mM KCl, pH7.4 at 7°C for 30min. |